Avec de nouvelles cibles de vaccination et des plateformes de livraison plus puissantes, les chercheurs font des percées vers un vaccin contre la grippe qui pourrait offrir une protection meilleure et plus durable.
Les chercheurs utilisent des nanoparticules pour construire des vaccins de grippe multi-antigènes comme celui illustré ici.Crédit d'image: Ian C.Haydon / UW Institute for Protein Design.
Lorsque les efforts de développement des vaccins de la maladie du coronavirus urgent (Covid-19) ont commencé sérieusement au début de 2020, les chercheurs ne se sont en aucun cas paru de zéro.Cela est en partie attribuable aux décennies de recherche dédiées à la création de meilleurs vaccins contre la grippe.En effet, de nombreux vaccinologues de la grippe ont pivoté à Covid-19 il y a deux ans, apportant pour porter les connaissances et les outils qu'ils avaient développés pour lutter contre une menace saisonnière qui a le potentiel de déclencher des pandémies.
Mais ces vaccinologues ne se sont pas détournés de leur objectif de longue date: un vaccin contre la grippe qui protège contre toutes les souches.Une telle réalisation pourrait sauver des centaines de milliers de vies chaque année.Et les efforts du vaccin Covid-19 peuvent finir par aider à accélérer ce travail.
Un vaccin contre la grippe universel représente un changeur de jeu qui pourrait prendre la menace de la grippe saisonnière et pandémique «hors de la table», selon un rapport de novembre 2021, l'un des quatre de la National Academy of Medicine (NAM) sur la façon de se préparer à unpandémie de grippe avec des leçons apprises de Covid-19.Tel que défini par le National Institute of Allergy and Infectious Diseases (NIAID) en 2018, un vaccin «universel» implique d'au moins 75% d'efficacité protégeant tous les groupes d'âge pendant au moins un an contre toutes les souches de grippe A (1).Idéalement, dit le rapport NAM, un vaccin universel pourrait également travailler contre la grippe B et offrir une protection pendant trois à cinq ans.
Les vaccins saisonniers contre la grippe - bien que des outils précieux à l'atténuation de la grippe - ne se produisent que la gamme étroite de souches qui sont les plus problématiques au cours d'une année donnée.Lorsque les projections sont désactivées, le décalage a conduit à une efficacité des vaccins aussi faible que 10%;Même dans une bonne année, l'efficacité du vaccin atteint à peine 60% (2).Il y a beaucoup en jeu: chaque année, la grippe entraîne environ 290 000 à 650 000 décès dans le monde malgré les vaccins saisonniers (3).Un nouveau virus de la grippe pour laquelle il n'y a pas de vaccin pourrait conduire à une pandémie qui tue des millions d'autres.
Un vaccin contre la grippe largement protecteur est un objectif depuis des décennies, mais il est devenu plus réalisable ces dernières années grâce à de nouvelles cibles de vaccination et à des plateformes de livraison plus efficaces.Lorsque le succès pandémique du coronavirus, les chercheurs en grippe faisaient déjà des progrès avec des plateformes telles que l'ARNm et les vecteurs viraux qui ont conduit à des vaccins à succès du coronavirus.
Tout cela signifie qu'il y a de bonnes raisons de croire qu'un vaccin universel de grippe est possible dans une décennie.Mais les obstacles restent - des réglementations conçues pour évaluer les vaccins contre la grippe plus traditionnels, à surmonter les bizarreries déroutantes du système immunitaire humain.
Une cible en mouvement
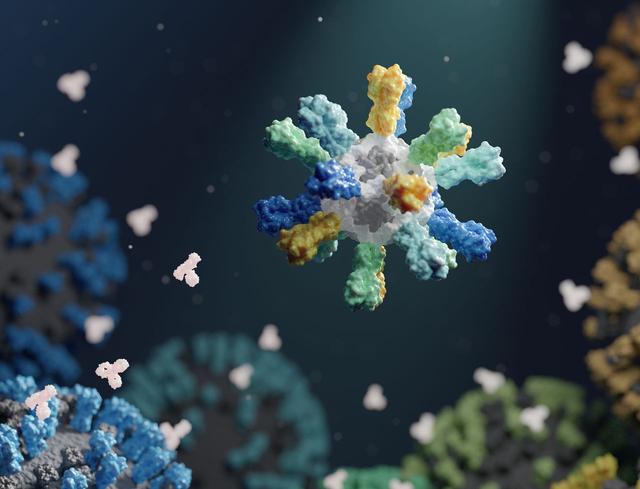
Une particule virale de la grippe ressemble beaucoup à l'image désormais tristement célèbre du coronavirus.Les protéines pointent vers l'extérieur à partir d'une sphère de lipides, formant une boule épineuse.La plus abondante de ces protéines saillantes est l'hémagglutinine, qui, avec une autre protéine de surface appelée neuraminidase, est l'endroit où les virus de la grippe A obtiennent leurs désignations «H» et «N» (voir fig.2).
L'hémagglutinine est la clé qui déverrouille les cellules hôtes, laissant le virus entrer.Cela en fait un objectif principal du système immunitaire humain et de la cible principale de la plupart des vaccins contre la grippe.Les vaccins contre la grippe visent à provoquer des réponses immunitaires à long et à court terme, y compris des anticorps qui reconnaissent des emplacements spécifiques sur l'hémagglutinine et se fixent à ces spots, bloquant le virus.
Mais l'hémagglutinine est une cible en mouvement.Il se compose d'une tige surmontée d'une tête qui est particulièrement sujette à évoluer, provoquant une accumulation de petits changements dans chaque déformation en circulation.Depuis les années 1970, l'Organisation mondiale de la santé a tenté de rester en avance sur ces changements en recommandant des mois à l'avance, lesquelles des souches circulantes à inclure dans les vaccins de grippe saisonnière (4).Ces dernières années, ces recommandations ont inclus deux souches de grippe A grippal A et de grippe B, qui sont toutes incorporées dans le seul vaccin «quadrivalent» donné aux États-Unis (5).
À la fin des années 2000, plusieurs groupes de recherche ont fait une découverte clé qui a suggéré qu'il pourrait être possible de mettre fin à la course contre les souches évolutives: les humains, il s'est avéré, peut générer des anticorps neutralisants contre la grippe contre des parties du virus qui restent largement inchangées (6).Depuis lors, la recherche était en cours pour le meilleur de ces régions «conservées».
Les virus contiennent de nombreuses protéines, toutes couvertes de sites antigéniques, ou épitopes, qui déclenchent des anticorps correspondants.Mais bien que frapper un site antigénique puisse porter le virus un coup mortel, frapper un autre peut le laisser relativement indemne."Votre système immunitaire ne connaît pas la différence entre ce qui est protecteur et ce qui ne l'est pas", explique l'immunologue Jenna Guthmiller, boursière postdoctorale à l'Université de Chicago, IL, et professeur adjoint entrant à l'Université du Colorado Anschutz Medical Campus à Aurora.La vaccination, dit-elle, peut enseigner à nos cellules B de génération d'anticorps pour se concentrer davantage sur l'attaque des régions critiques du virus.Mais vous devez d'abord attirer l'attention des cellules.
Rediriger l'attention
De nombreux chercheurs développant des vaccins contre des parties conservées du virus de la grippe se sont concentrées sur la tige de l'hémagglutinine, qui change généralement moins que la tête.Malheureusement, la tige ne génère pas une réponse immunitaire aussi forte.La raison de «l'immunodominance» du chef n'est pas entièrement claire, explique le virologue et vaccinologue Florian Krammer de l'École de médecine Icahn à Mount Sinai à New York.
Mais Krammer, ainsi que les collègues collaborateurs virologues, développe des protéines d'hémagglutinine qui attirent l'attention du système immunitaire sur la tige.Ils le font en profitant d'une autre tendance du système immunitaire: répondre le plus facilement à ce qu'il sait déjà.Même les souches incluses dans les vaccins de grippe saisonnières d'année en année, qui peuvent avoir des têtes d'hémagglutinine suffisamment différentes pour échapper aux anticorps adaptés à une version passée, incluent également bon nombre des mêmes sites antigéniques similaires.Ainsi, la tête est à la fois immunodominante et très familière.«Le domaine de la tête présente tous les avantages», explique Krammer.
Le groupe de Krammer prend une protéine d'hémagglutinine et échange la tête familière pour une à une souche éloignée.La tête de cette hémagglutinine chimérique est toujours immunodominante, mais la tige est la seule partie familière.«Donc, vous redistribuez les avantages», explique Krammer.En livrant une deuxième vaccination avec la même tige et une autre tête inconnu, l'avantage de la tige grandit.
L'équipe a récemment conçu un vaccin pour protéger contre les virus de la grippe A du groupe 1 - l'un des deux groupes dans la grippe A basé sur la parenté de leurs hémagglutinines (7).Pour faire de la tige H1 la cible la plus familière présentée dans le vaccin, ils ont dépassé leurs hémagglutinines chimériques avec des têtes des virus aviaires H5 et H8.Les résultats de leur essai clinique de phase 1, publié en janvier 2021, ont montré que le vaccin a induit une large réponse immunitaire durable contre la tige (8).L'équipe développe de la même manière des vaccins pour se protéger contre les virus de la grippe A Group 2 plus éloignés et contre la grippe B, dans le but ultime de créer un vaccin universel de grippe universel trivalent.
Malgré beaucoup de potentiel dans la tige, la tête peut être prometteuse encore, dit Guthmiller.Elle a récemment isolé des anticorps produits par des volontaires vaccinés contre le virus H1N1 2009.La virologue structurelle Julianna Han du Scripps Research Institute de La Jolla, en Californie, a ensuite utilisé la microscopie électronique pour révéler précisément comment et où chaque anticorps s'attachait à la tête de l'hémagglutinine.Sur les 66 anticorps individuels identifiés, les régions de tête conservées entièrement ciblées (9) (9).Dans une étude in vitro, ces anticorps ont bloqué presque tous les virus H1N1 humains.Et chez la souris, un échantillon représentatif des anticorps a fourni une protection à 100% contre la perte de poids et la mort d'un virus H1N1 adapté à la souris.
D'autres apportent une force brute de calcul à la recherche des meilleurs épitopes dans le but de «construire» une meilleure hémagglutinine pour une utilisation comme antigène vaccinal (10).Le vaccinologue Eric Weaver, directeur du Nebraska Center for Virology de l'Université du Nebraska - Lincoln, Mines Public Databases pour collecter les données de séquence de gènes de l'hémagglutinine pour les souches de grippe enregistrées au fil du temps.Lui et son équipe entrent dans ces données dans le concepteur de vaccins épigraphiques, un algorithme informatique qui construit une nouvelle hémagglutinine basée sur les variations les plus courantes de la structure de la protéine.Pour combler les lacunes potentielles dans la protection, l'algorithme peut créer une autre protéine d'hémagglutinine en utilisant les formes les plus fréquentes de chaque région variable non capturée dans la première protéine, et ainsi de suite pour des conceptions supplémentaires.
Travaillant dans des porcs, qui peuvent servir de vaisseaux de mélange pour les souches aviaires, humaines et de porcs pour échanger des segments de génome, l'équipe de Weaver a récemment développé un vaccin visant à protéger les porcs nordporcs (11).Les porcs vaccinés avec un mélange de trois protéines d'hémagglutinine synthétiques ont généré des anticorps qui protégeaient contre 11 des 13 souches de porcs H3 nord-américaines testées."Si nous pouvons protéger les porcs contre les humains, et si nous pouvons protéger les humains des porcs", dit Weaver, "nous éliminerons ce navire de mélange."
Plus que l'emballage
Aux États-Unis, la plupart des vaccins antigrippaux contiennent des virus de la grippe inactivés ou affaiblis, ce qui peut nécessiter des doses élevées pour générer une réponse immunitaire suffisante (12).Mais comme les chercheurs révèlent de nouvelles cibles vaccinales plus spécifiques, ils constatent également que la plate-forme vaccinale elle-même - la façon dont un antigène est livré au corps - peut avoir d'énormes impacts sur la force et la qualité des réponses immunitaires à ces cibles.
Lynda Coughlan, vaccinologue à la University of Maryland School of Medicine de Baltimore, développe des vaccins qui exploitent un autre virus en tant qu'outil de livraison (13).Les adénovirus infectent naturellement les humains, provoquant une gamme de maladies (14). Researchers can turn these adenoviruses into a “vector" for flu vaccines by deleting the genes that allow the adenoviruses to replicate.À l'intérieur de cette coquille virale, les chercheurs insèrent des séquences d'ADN codant pour les antigènes de la grippe qu'ils souhaitent présenter.
Un grand avantage de ces virus d'ADN en tant que vecteurs de vaccin est qu'ils utilisent la propre machinerie de transcription et de traduction du receveur des vaccins pour générer la protéine antigène.Et, en principe, le vaccin peut continuer à produire de l'antigène pendant des semaines ou plus, qui, selon les chercheurs, pourrait prolonger la réponse immunitaire (15).De plus, la façon dont ces vecteurs pénètrent dans les cellules plus étroitement imite certaines infections virales réelles, qui engagent plus activement le système immunitaire.
COVID-19 vaccines currently on the market produced by AstraZeneca, China’s CanSino Biologics, Russia’s Gamaleya Institute, and Janssen (Johnson & Johnson) also use this adenoviral-delivery strategy, although interest in the technology long predates the pandemic.Le Jenner Institute de l'Université d'Oxford (Royaume-Uni), où les chercheurs ont développé le vaccin contre le covid-19 de l'AstraZeneca, a testé son vecteur d'adénovirus de chimpanzé contre une gamme de maladies, y compris la grippe, bien qu'aucun n'ait fait sur le marché jusqu'à ce que le vaccin covide soit covide.Coughlan dit que l'ensemble précédent avec l'utilisation de vaccins à vecteur d'adénovirus contre Covid-19 chez l'homme peut aider à ouvrir la voie au champ de grippe. And despite safety issues raised by the Centers for Disease Control and Prevention (CDC) in December regarding Johnson & Johnson's adenovirus-based COVID-19 vaccine as compared with mRNA products,* Coughlan says she’s confident that researchers can make modifications to adenoviral vectors to increase safety in the future.
Dans une étude récente, Coughlan et ses collègues du mont Sinaï et d'autres institutions ont créé un vaccin qui a déclenché la production de la protéine d'hémagglutinine à partir du virus H1N1 2009;il protégeait les souris de cette souche (16).Ils ont également testé si ce vaccin adénoviral protégeait des souris exposées à un autre virus - celle avec une tige qui correspondait à l'antigène hémagglutinine dans le vaccin mais une tête entièrement différente.Toutes les souris ont survécu, explique Coughlan, par rapport à seulement quelques animaux qui ont reçu un vaccin H1N1 traditionnel.Lorsque l'équipe a répété l'expérience avec un virus encore plus éloigné, la différence était encore plus austère.Les souris vaccinées adénovirales ont survécu, alors qu'aucun des autres ne l'a fait (16).
Messenger RNA (ARNm), une plate-forme maintenant célèbre pour son utilisation dans les vaccins Moderna et Pfizer-BionTech Covid-19 et les puissantes réponses immunitaires qu'ils induisent, était également en développement par ces sociétés en tant que vaccin contre la grippe avant le hit pandémique du coronavirus (17, 18).
Le succès des vaccins contre le coronavirus d'ARNA témoigne de la façon dont la plate-forme peut fonctionner, explique le vaccinologue Norbert Pardi de l'Université de Pennsylvanie à Philadelphie, qui en 2015, ainsi que les pionniers du vaccin contre l'ARNA, Katalin Karikó et Drew Weissman, et d'autres, ont démontré que l'emballageL'ARNm dans un revêtement protecteur des lipides l'empêche de dégrader trop rapidement et l'aide à entrer dans les cellules (19).
La technologie des vaccins d'ARNm permet aux chercheurs d'échanger rapidement un codage d'ARNm contre différents antigènes et d'inclure plusieurs antigènes à la fois.Dans une étude en 2020, Pardi, Coughlan et d'autres ont testé un vaccin d'ARNm qui combinait quatre protéines de grippe.L'une de ces protéines était une hémagglutinine spéciale qui ne contenait que la tige - une autre stratégie pour diriger la réponse immunitaire loin de la tête.De plus, l'équipe a inclus la neuraminidase et deux autres protéines virales qui ont tendance à être plus conservées.L'idée est que l'incorporation de plusieurs cibles offre une protection plus large et aide également les paris haies.Si l'une de ces régions virales évolue pour échapper au système immunitaire, explique Pardi, les autres cibles pourraient toujours offrir une protection.
Les souris protégées par le vaccin d'un large éventail de virus de la grippe A du groupe 1 (20) (20).En fin de compte, l'équipe prévoit d'inclure environ 10 à 12 antigènes couvrant la grippe A et B. “This is how we believe that we can really develop a globally protective vaccine," says Pardi.
D'autres combinent également plusieurs cibles d'antigène dans de nouvelles plates-formes dans le but de remonter à la fois l'étendue et la force de la réponse immunitaire.Les chercheurs du Niaid’s Vaccine Research Center (VRC) à Bethesda, MD, utilisent des nanoparticules pour construire des vaccins de grippe multi-antigènes (voir Fig.1). It’s a “very strong way to stimulate the immune system," says VRC vaccine immunologist Masaru Kanekiyo.
La protéine la plus abondante dépassant du virus de la grippe est l'hémagglutinine, qui sert de clé qui déverrouille les cellules hôtes, laissant le virus entrer.La protéine d'hémagglutinine de la grippe est la principale cible de la plupart des vaccins contre la grippe.Mais la protéine évolue constamment, surtout dans sa région de la tête.Crédit d'image: réimprimé avec la permission de Ref.9, https: // www.la science.org / doi / 10.1126 / SCITRANSLMED.ABG4535.
L'équipe conçoit une séquence génétique codant pour un antigène plus une pièce nanoparticule à une extrémité.Ils mélangent ensuite cette nouvelle protéine avec une autre pièce de nanoparticules dont la forme est complémentaire au premier. The nanoparticles click into place like a three-dimensional puzzle, forming an “immunogen" sphere with antigens pointing outward.
Dans un test récent, Kanekiyo et collaborateurs ont montré qu'une nanoparticule vaccinale affichant un total de 20 copies de quatre protéines d'hémagglutinine - une de chacune des souches dans un vaccin contre la grippe saisonnière - a généré de fortes réponses immunitaires dans plusieurs modèles animaux contre ces souches spécifiques égalementcomme ou mieux que le vaccin commercial (21).Mais le vaccin contre les nanoparticules a également offert une plus grande protection contre les souches de grippe plus éloignées, y compris les souches aviaires avec un potentiel pandémique.
Kanekiyo soupçonne que l'espacement physique entre les antigènes dans la nanoparticule peut créer une structure qui frappe dans la «zone de frappe du système immunitaire." Whatever the mechanism, the nanoparticle platform seems to enhance the immune response, while also directing attention to the hemagglutinin stalks.L'équipe teste actuellement un vaccin similaire dans un essai clinique de phase 1.
Comprendre les différents types de réponses immunitaires induites par différentes plateformes de vaccins est un grand domaine de recherche, explique Coughlan.Les essais avec des vaccins Covid-19 ont démontré que le mélange et la correspondance de différentes plateformes peuvent offrir les avantages de chacun tout en renforçant les réponses globales (22).Coughlan envisage qu'un vaccin contre la grippe vraiment universel peut nécessiter de la même manière plusieurs plateformes. People might, for example, receive a two-shot “universal" flu vaccination with an adenoviral-based “prime" and then an mRNA “boost."
Péché original et autres obstacles
Malgré ces avancées, la formule gagnante d'un vaccin universel de grippe est loin d'être certain.Le rapport NAM indique qu'il «reste un problème scientifique difficile sans garantie qu'un vaccin peut être développé qui fournira une protection à long terme chez les personnes de tous les groupes d'âge» (23).
One major challenge is posed by a phenomenon sometimes called “original antigenic sin," or imprinting (24).Pour des raisons qui ne sont toujours pas totalement claires, la réponse immunitaire à toute souche de grippe est lancée en grande partie par les mêmes cellules B qui se sont développées lors de la première exposition à la grippe d'une personne, même lorsque la souche est dépareillée (à moins que la nouvelle souche soit si significativement différenteque c'est au-delà de la reconnaissance).Guthmiller dit que ce n'est pas que les expositions ultérieures n'ont pas d'importance;Elle aime imaginer une pyramide, chaque exposition ajoutant un autre niveau, bien que les cellules B de cette première exposition - le fondement de la pyramide - restent les plus dominantes.
Une étude récente de Guthmiller, Coughlan, Krammer et d'autres suggère que la vaccination peut influencer davantage le système immunitaire vers la génération d'anticorps protecteurs, tandis que l'infection a tendance à entraîner des anticorps plus protecteurs liés à une infection infantile (25).Mais il reste à voir à quel point les candidats vaccinaux universels se produiront dans un grand nombre de personnes qui ont des antécédents d'exposition uniques.Sur la base de ce que nous savons en ce moment, Han dit: «Même si vous essayez d'élargir la réponse d'un individu à plusieurs souches de grippe, vous ne pouvez vous rendre si loin que sur les biais déjà présents dans le système immunitaire de cet individu." One possible workaround, she suggests, might be to develop different universal flu vaccines for different age groups.
Another wildcard is durability—both in terms of how long vaccine-induced immune memory will remain active, and how long a particular vaccine formulation remains “universal" enough. “In a perfect world, you would get vaccinated at the age of six months or one year and then you wouldn’t need it again until you were 50," says Weaver.«Il est plus probable que l'évolution continuerait de se produire et que celles-ci devraient être mises à jour."
Étant donné qu'un vaccin contre la grippe qui est à la fois durable, largement protecteur et très efficace pourrait s'avérer un stade de haute, au moins à court terme, Coughlan voit également une place pour un vaccin qui pourrait limiter la gravité de la maladie pour une large gammedes souches de grippe - même si cela n'empêche pas l'infection.Ce vaccin contre les arrêts pourrait être lyophilisé, stocké et déployé uniquement en cas de pandémie. “You want people to have some level of protective immunity, even if it’s not perfect, as quickly as possible without the lag phase of waiting for manufacturing of a perfectly matched vaccine," she says.
Les vaccins universels contre la grippe pourraient faire face à des obstacles régulateurs (26).La plupart des candidats seraient suffisamment différents des vaccins saisonniers existants, ce qui signifie que les approuver dans le cadre des directives réglementaires actuelles nécessiteraient plus que la simple montre que les soi-disant corrélations de protection;Les développeurs de vaccins devraient effectuer l'étape supplémentaire pour démontrer que le vaccin empêche les gens de tomber malade, explique Krammer.«Cela pourrait être la différence de plusieurs millions de dollars dans le coût de l'essai clinique."
Mais Momentum est en train de se construire et le rythme de la découverte peut augmenter avec un nouveau financement pour des efforts comme les centres d'innovation de vaccin contre la grippe de NIAID (civique).Lancé à l'automne 2019, Civics Support Collaborative Research, Vaccin Manufacturing et Clinical Trials, tous dans les installations du réseau civique. “I think that a lot of interesting vaccine approaches will come out of that structure," says Krammer, who is co-principal investigator for one of three vaccine research centers within the network.
Comme de nombreuses recherches sur la grippe, le travail précoce de la civique a été ralenti par les problèmes de pandémie de coronavirus et de chaîne d'approvisionnement. “That has impacted a lot of lab work," says Krammer, adding that many influenza researchers—including himself—also shifted their attention to the new coronavirus for a time.
Pourtant, il espère que la pandémie du coronavirus pourrait encore jouer un rôle dans l'avancement d'un vaccin universel de grippe, à la fois en renouvelant l'enthousiasme public pour les vaccins et en démontrant combien peut être accompli avec suffisamment de volonté politique et de soutien financier. “The public learned that pandemics happen and we need to be prepared," says Krammer—but, he adds, researchers in the flu field “didn’t need that reminder."
Notes de bas de page
Cet article est distribué sous Creative Commons Attribution-Noncommercial-Noderivatives Licence 4.0 (CC BY-NC-ND).